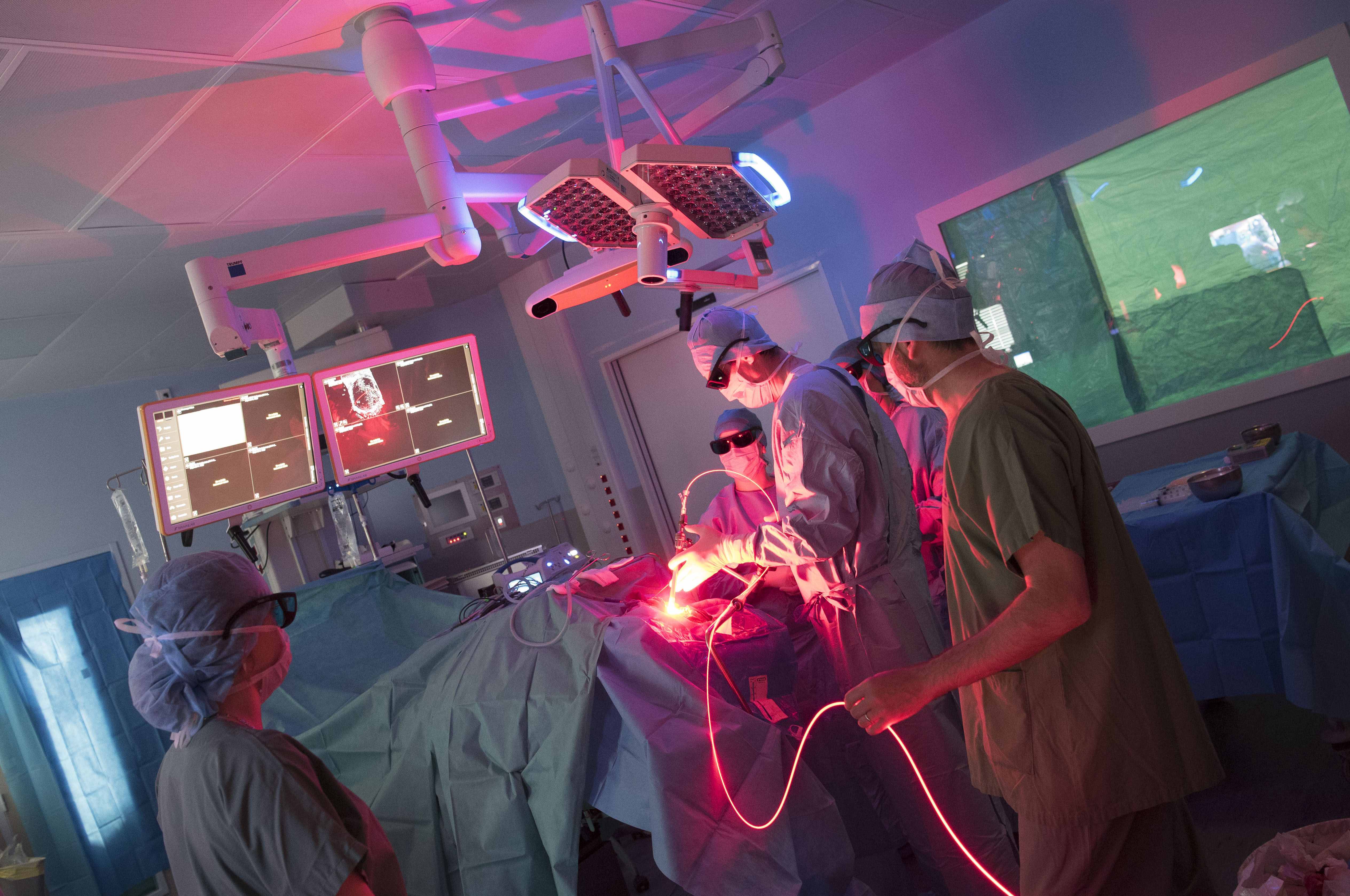
Etude de Phase 1 de thérapie photodynamique peropératoire du glioblastome |
En cours / clôturé : Actif (recrutement terminé, suivi des patient.es) |
|
Type de recherche (rétro/prospectif) : prospectif |
|
Synopsis : Le glioblastome, tumeur cérébrale primitive maligne la plus fréquente chez l’adulte, avec une incidence en France de 4/100 000. La médiane de survie est de 14,5 mois avec le traitement standard (chirurgie, radio-chimiothérapie). Les récidives surviennent donc dans un premier temps essentiellement au niveau des berges tumorales. Il a été démontré dans de nombreuses études que la qualité de l’exérèse chirurgicale est un facteur pronostic majeur. Ainsi, l’optimisation du contrôle local demeure un enjeu significatif afin d’améliorer la survie sans progression et la survie globale. Dans ce contexte un nouveau traitement focal, complémentaire de l’exérèse chirurgicale, tel que la thérapie photodynamique (PDT), est à évaluer. La thérapie photodynamique consiste en l’administration d’un photosensibilisateur (PS), qui après accumulation préférentielle dans les cellules tumorales, est activé par illumination à une longueur d’onde spécifique. L’acide-5-aminolévulinique (5-ALA) a déjà l’AMM en France pour la neurochirurgie fluoroguidée (Gliolan®, Medac, Allemagne). Le 5-ALA est précurseur, dans le cycle de l’hème, de la protoporphyrine IX (PpIX) qui s’accumule de façon très préférentielle dans les cellules de glioblastome et constitue le photosensibilisateur. L’illumination à une longueur d’onde spécifique des cellules chargées de PpIX entraîne la formation d’agents oxygénés cytotoxiques. Cela constitue le principe de la PDT. La PDT peut être utilisée en conditions per-opératoires par illumination de la cavité après exérèse maximale (« per-PDT » ou « intraoperative PDT »). A notre connaissance, aucun essai de per-PDT 5-ALA n’a été mené à ce jour. Un tel essai est donc une perspective innovante, le 5-ALA étant très prometteur dans la littérature, à la fois sur le plan de l’efficacité et sur le plan de la tolérance. Nous proposons un essai clinique de phase I monocentrique au CHRU de Lille, pour évaluer la faisabilité d’un protocole de per-PDT médiée par 5-ALA-PPIX, chez des patients atteints de glioblastome accessible à une exérèse chirurgicale complète de la prise de contraste. Ce traitement sera réalisé en complément du traitement de référence actuel du glioblastome : chirurgie d’exérèse maximale puis radiochimiothérapie selon le protocole Stupp. Le critère principal sera la faisabilité, évaluée par la proportion de patients ayant pu faire l’objet d’une PDT per opératoire au cours de la chirurgie d’exérèse du glioblastome, sans toxicité inacceptable. L’objectif attendu est de 70%, soit 7 patients sur les 10 que nous prévoyons d’inclure. Les critères secondaires de jugement seront la survie sans progression (SSP), la survie globale, et l’évaluation à 3 mois, 6 mois et 12 mois de la réponse radiologique au traitement, ainsi que la qualité de vie des patients. |
|
Principal·e investigateur·rice : Pr Nicolas REYNS (Service de Neurochirurgie, Hôpital Salengro) |
|
Scientifique coordinateur·rice : Dr. Maximilien Vermandel (Université de Lille - France) - Pr. Serge Mordon (INSERM - France) |
|
Sponsor de l’étude : CHU de Lille |
|
Objectif principal : Evaluer la faisabilité de la réalisation de la PDT per opératoire au cours de la chirurgie d’exérèse du glioblastome, sans toxicité immédiate inacceptable. |
|
Objectifs secondaires :
|
Critère d’évaluation primaire : Proportion de patients ayant pu faire l’objet d’une PDT per opératoire au cours de la chirurgie d’exérèse du glioblastome sans évènement indésirable grave (objectif attendu : 70%) |
|
Critères d’évaluation secondaires :
|
Recrutement estimé : 10 patient.es |
|
Identifiant clinicaltrials.gov : NCT03048240 |
|
Contact et localisation : CHU de Lille
|